Publié le 23 juin 2013Lecture 9 min
Les angio-œdèmes non histaminiques
M. VIGAN, UF Allergologie, Département de dermatologie, CHU de Besançon
Les angio-oedèmes non histaminiques doivent être connus des dermatologues. D’une part, ils sont une cause non négligeable de consultation et leur méconnaissance, en particulier par confusion avec les AO histaminiques, peut faire courir au patient un risque vital. D’autre part, parce que la compréhension de leur physiopathologie a permis de codifier leur prise en charge, qui s’est nettement améliorée dans les dix dernières années.
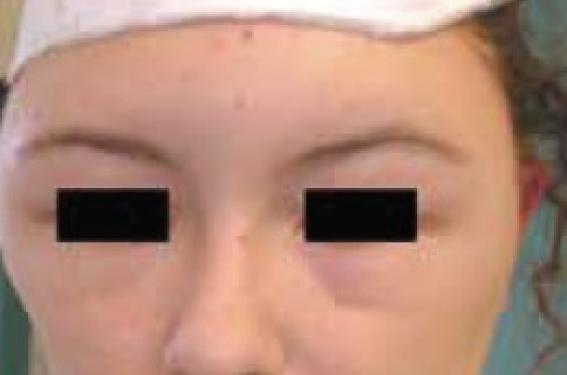
Définition Un angio-oedème (AO) est un oedème sous-cutané, soudain, transitoire et récidivant plus ou moins fréquemment. Il se développe en quelques heures et cède spontanément. Il s’agit d’un oedème fonctionnel disparaissant sans séquelle, dont l’histologie ne montrerait aucune lésion spécifique. Cette définition exclut les aspects oedémateux qui s’aggravent progressivement, avec histologie spécifique ou non, comme par exemple l’oedème observé dans le syndrome cave supérieur. Les AO sont différents des oedèmes par déclivité dus à un eczéma aigu du cuir chevelu par exemple (figure 1/illustration). Figure 1. Œdème du visage associé à un eczéma aigu du cuir chevelu suite à une teinture capillaire chez une patiente présensibilisée par un tatouage éphémère noir, prédominant sur la partie haute du visage et dû à la déclivité : ce n’est pas un angio-œdème à bradykinine. En fonction du médiateur impliqué, on distingue (tableau 1) : – les AO histaminiques ; – les AO non histaminiques, avec principalement les AO à bradykinine. Les angio-œdèmes à bradykinine (AOBK) Physiopathologie des AOBK La bradykinine (BK) est un puissant vasodilatateur, qui a un rôle protecteur cardiaque. En cas de production trop importante ou de trouble de la dégradation, la BK est responsable de l’augmentation de la perméabilité vasculaire avec œdème local massif et incontrôlé, d’une contraction des muscles lisses et de douleur. La production de BK se fait au niveau de la cellule endothéliale : le stress endothélial, par modification de la polarisation et du pH, active le facteur XII qui à son tour active les autres kininogénases : la plasmine et la prékallicréine. Cette dernière, transformée en kallicréine, associée à la plasmine activée, va transformer le kininogène en BK ; celle-ci est dégradée par des enzymes spécifiques (kininases), dont le plus connu est inhibiteur de l’enzyme de conversion de l’angiotensine (ECA), en différents métabolites inactifs, en dehors de la Des-Arg BK. La durée de vie de la BK est très courte. Lorsqu’elle peut se fixer sur son récepteur β2 constitutionnel, ou si par trouble de son catabolisme, la Des-Arg BK se fixe sur le récepteur β1 inductible, l’oedème apparaît. La seule régulation connue de la phase des kininogènes est l’inhibiteur de la C1 estérase (C1 Inh). Des facteurs génétiques peuvent dans certains cas être impliqués(1,2). Il est possible de classer les AO à BK en référence à l’anomalie de C1 Inh (tableau 2) ou en référence aux facteurs génétiques (tableau 3). Clinique des AOBK L’aspect clinique de l’AOBK est constant quelle que soit sa place dans les différentes classifications. Le dermatologue doit en connaître les signes cutanés, et rechercher par l’interrogatoire les signes extracutanés, en gardant en tête que le pronostic vital est lié à l’AO laryngé, responsable de décès dans plus de 25 % des cas si, le diagnostic n’étant pas fait, le traitement adapté n’est pas mis en place à temps. Signes cutanés Il s’agit d’un œdème sous-cutané ou sous-muqueux, blanc, mou, non prurigineux, non inflammatoire (pas chaud), survenant par crises, disparaissant en 2 à 5 jours, sans séquelle. Il s’agit souvent d’un fait clinique rapporté par le patient lors d’une consultation, et il est important d’obtenir une photo clinique au moment où les lésions sont les plus visibles (figure 2). Classiquement, la zone atteinte est constante pour un même patient, mais elle varie d’un patient à l’autre : organes génitaux externes, bras, jambe, visage, main, doigt. Les antihistaminiques et les corticoïdes pris en début d’évolution sont inefficaces(3). Figure 2. Cette photo prise par le mari de la patiente objective un angio-œdème à bradykinine déformant à sa phase aiguë. Signes digestifs Les crises douloureuses abdominales peuvent être isolées. Elles induisent une laparatomie exploratrice dans un tiers des cas avec le risque opératoire que cela implique. Elles sont pseudo-occlusives, et représentent une pseudo-urgence chirurgicale. Elles se caractérisent par une douleur intense (EVA = 10), dans 69 % des cas, associée à une contracture abdominale et des vomissements dans 73 % des cas. L’arrêt des matières et des gaz, suivi d’une débâcle diarrhéique est possible, associée à une ascite plus ou moins massive qui mérite d’être objectivée tout comme l’oedème muqueux par l’imagerie (scanner, échographie). Un choc hypovolémique est possible (5 % des cas). Les crises douloureuses abdominales peuvent être isolées, particulièrement chez l’enfant. Les autres signes Les voies aériennes supérieures peuvent être atteintes : détresse respiratoire par oedème sous-glottique (25 % des œdèmes laryngés non traités sont fatals). Le début est progressif : dysphonie, respiration bruyante, dysphagie. La dyspnée laryngée s’accompagne d’un risque d’asphyxie pouvant nécessiter une trachéotomie. L’œdème laryngé est parfois provoqué par des soins dentaires et un œdème de la face, et il est une complication redoutée des AO par IEC. Ces derniers doivent être arrêtés devant tout AO et ne doivent pas être réintroduits. Des cystalgies, des céphalées, une impression d’ébriété sont souvent rapportées par les patients. Diagnostic des AOBK Il est fondé sur des notions d’épidémiologie : les AO héréditaires (AOH) type I et II (tableaux 2 et 3) autosomiques dominants, concernent 1/50 000 à 100 000 habitants en France (500 personnes environ) ; les AO acquis non médicamenteux sont encore plus rares. Les angio-oedèmes dus aux IEC touchent 0,2 % des patients traités par IEC, avec une incidence de 1,97 cas/1 000 patients testés/an, et surviennent surtout dans la population noire et chez la femme. Le diagnostic est bien codifié pour les AOH de type I et type II, en sachant que le type I représente 85 % des cas d’AOH. Il repose sur des critères cliniques et biologiques. Le diagnostic des AOH de type I et II se fait sur l’association de deux critères majeurs cliniques et un critère biologique (tableau 4). Il est plus difficile pour les AOH de type III : ils peuvent être associés à une anomalie de fonction de C1 Inh (qui se normalise à l’arrêt des estrogènes) et des kininogénases ; mais la clinique, les éventuels cas familiaux, l’efficacité de l’arrêt des estrogènes et de l’acide tranexamique sont déterminants. Le diagnostic des AO acquis non médicamenteux par consommation ou par neutralisation du C1 Inh se fait sur le dosage de la fonction plus que sur le dosage pondéral de C1 Inh. Le diagnostic des AO acquis médicamenteux se fait sur l’association du tableau clinique et des poussées d’AO. Le sexe féminin et la peau noire sont des facteurs de risque des AO aux médicaments. Les AO surviennent dans 55 % des cas dans les 90 jours suivant le début du traitement, et donc dans 45 % des cas bien après. Les AO dus aux IEC sont paroxystiques, ils peuvent s’aggraver au fils du temps : tout AO sous IEC doit conduire à les arrêter. Prise en charge thérapeutique Les cibles du traitement peuvent être la phase d’activation de la plasmine (acide tranexamique), la production du C1 Inh par le foie (Danatrol®), le taux de C1 Inh (concentré de C1 Inhibiteur), le récepteur β2 de la bradykinine (Icatiban®). Il est nécessaire de respecter les contre-indications notées sur le Vidal® et de respecter les consignes indiquées au tableau 5. Une carte décrivant l’affection est remise au patient. • Le traitement des AOH de type I et II est bien codifié (figure 3). Les critères de sévérité sont les suivants : antécédents d’oedème laryngé ou de la face, soins dentaires, âge entre 11 et 45 ans. • Le traitement des crises des autres AOBK est semblable à celui des AOH. • Le traitement de fond de l’AOH de type III consiste à arrêter les estrogènes, à proposer une contraception non hormonale ou par un progestatif, tel le nomégestrol acétate, et si l’oedème persiste, à appliquer le traitement des AOH de type I et II. • Le traitement des AO acquis non médicamenteux, en dehors de ceux cités plus haut a pour particularités la possibilité de traiter la maladie associée par corticoïdes ou médicaments adaptés, en cas d’hyperconsommation, et d’utiliser de très hautes doses de C1 Inh et des auto-anticorps (rituximab) en cas de déficit par neutralisation. • Les AO acquis par IEC impliquent l’arrêt définitif des IEC. Les oedèmes sous sartans sont liés au récepteur AT2 ; le taux de réactions aux IEC associées aux réactions aux sartans semble suffisamment faible pour que ces médicaments puissent être prescrits après un AO aux IEC(4). Figure 3. Traitement de l’angio-œdème héréditaire. Conclusion Les angio-œdèmes non histaminiques, et particulièrement les AO à bradykinine doivent être bien connus des dermatologues. Ces derniers doivent savoir : – arrêter les IEC en cas d’AO acquis, évoquer les autres AO sur l’aspect clinique (les photos numériques sont très intéressantes), et évolutifs sous traitement par acide tranexamique ; – orienter leurs patients vers un centre de compétence pour confirmer le diagnostic et faire les enquêtes génétiques ; – accompagner les patients et leur médecin traitant dans la conduite du traitement et des actes de prévention(5).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :