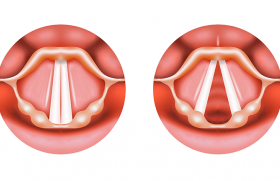
Laryngologie
Publié le 27 fév 2024Lecture 9 min
Prise en charge du reflux laryngopharyngé
François BOBIN, ORL, Poitiers
Le reflux laryngopharyngé (RLP) est une pathologie inflammatoire de la muqueuse des voies aéro-digestives supérieures liée à l’action directe ou indirecte du reflux du contenu gastrique, s’accompagnant de modifications morphologiques(1). La prévalence des symptômes associés au RLP est estimée à 15 à 30 % des patients consultant en ORL et 50 % des consultations de phoniatrie(2). Son expression clinique polymorphe et non spécifique rend sa prise en charge difficile, d’autant que les examens paracliniques le concernant sont peu diffusés en France.
RAPPEL PHYSIOPATHOLOGIQUE
(figure 1)
Figure 1. Rappel physiopathologique. Le RLP peut être d’origine gastrique (HCL et pepsine) et/ou pancréatique (sels biliaires, enzymes pancréatiques) par reflux duodéno-gastrique associé.
La classification de consensus de Montréal (2006) place le RLP dans les associations établies extra-œsophagiennes du reflux gastro-œsophagien (RGO)(3). La première publication d’atteinte laryngée du reflux, l’ulcère de contact, date de 1968(4). Malgré sa prévalence, le RLP n’est connu de façon satisfaisante que par 27 % des ORL français(5).
En effet, le RLP est polymorphe dans sa physiopathologie comme dans son expression clinique. Il peut être acide ou peu/non acide, liquide ou gazeux, il peut contenir des enzymes protéolytiques comme la pepsine, qui peut induire des lésions directes sur la muqueuse laryngopharyngée(6). Il peut s’associer ou non à un RGO. Son expression symptomatique dépend du régime alimentaire(7), du niveau de stress(8), lequel est lié au système nerveux autonome. Les signes fonctionnels et d’examen, pris séparément, sont peu spécifiques et peuvent être rencontrés dans d’autres pathologies des voies aérodigestives supérieures, mais des outils diagnostiques cliniques et paracliniques permettent depuis peu de mieux appréhender le RLP.
DIAGNOSTIC CLINIQUE DU RLP
Les signes fonctionnels les plus fréquents, dont aucun n’est spécifique, sont liés à l’inflammation de la muqueuse (dysphagie, brûlures pharyngées, douleurs), à l’hypersécrétion de mucus (rhinorrhée postérieure, hemmage, toux sèche), à l’œdème muqueux (sensation de corps étranger pharyngé, globus) tandis que l’enrouement associe de façon plus complexe des modifications histologiques et biomécaniques des plis vocaux.
La raucité/dysphonie liée au RLP peut être causée par différents mécanismes au niveau laryngé incluant la réduction de la sécrétion des ions bicarbonates, la présence de mucus épais (lié à la réduction de l’expression de la mucine), la déhiscence intercellulaire laquelle favorise les microtraumatismes muqueux cordaux lors de vibration des plis vocaux. D’autres lésions peuvent être favorisées par le RLP et la réduction des divers mécanismes de défense muqueux par la pepsine tels que les ulcérations, les granulomes, les kératoses, et les dysplasies. Le RLP pourrait être associé à un assèchement de l’espace de Reinke et un infiltrat inflammatoire de ce dernier.
QUESTIONNAIRES ET SCORES DU RLP
Questionnaire patient RSS (Reflux Symptom Score/2018-2021)
(figure 2)
Figure 2. RSS-112 (Reflux Symptom Score). Le RSS-12 (2021) comprend 12 items : 7 items ORL, 3 items digestifs et 2 items respiratoires. Le RSS-12 se calcule en multipliant pour chaque item les scores de fréquence et de sévérité puis en additionnant les produits obtenus. Il est positif lorsque le total est supérieur à 11. Le score de qualité de vie valide les réponses du patient. Le RSS-12 est une aide au diagnostic et un outil de suivi évolutif.
Des questionnaires ont été développés pour hiérarchiser les symptômes, comme le RSI (Reflux Symptom Index) en 2002, avec 9 items dont un seul digestif, et plus récemment en 2018 le RSS (Reflux Symptom Score) avec deux versions : une à 22 items(9) et une à 12 items(10) (RSS-12). Ce dernier, plus rapide à utiliser, se compose de 7 items ORL, 3 items digestifs et 2 items respiratoires. Le RSS et le RSS-12 se calculent en multipliant pour chaque item les scores de fréquence et de sévérité puis en additionnant les produits obtenus.
Le RSS-12 est positif lorsque le total est supérieur à 11 tandis que le RSS est positif lorsque le score total est supérieur à 13.
Un score de qualité de vie, validant les réponses du patient, peut également être calculé.
Score d’examen clinique RSA (Reflux Sign Assesment, 2019)
(figure 3)
Figure 3. RSA (Reflux Sign Assesment). Le RSA (2018) combine les signes oraux, pharyngés et laryngés. Il comprend 17 items cotés entre 2 et 5 : 3 items pour la cavité buccale, 5 pour le pharynx, 9 pour le larynx. Le RSA est positif lorsque le score est supérieur à 14.
Les signes d’examen clinique sont également peu spécifiques et des scores ont été proposés pour les quantifier. Le RFS (Reflux Finding Score, 2001), limité aux seuls signes laryngés, est peu significatif, c’est pourquoi nous avons développé le RSA(11) (Reflux Sign Assesment, 2019), lequel combine les signes oraux, pharyngés et laryngés. Il comprend 17 items cotés entre 2 et 5 : 3 items pour la cavité buccale, 5 pour le pharynx, 9 pour le larynx.
Le RSA est positif lorsque le score est supérieur à 14.
DIAGNOSTIC PARACLINIQUE DU RLP
pH-impédancemétrie œsophagienne des 24 heures(12)
(figures 4 et 5)
Figure 4. pH-impédancemétrie œsophagienne des 24 heures (pHi). Sonde et boîtier enregistreur en place.
Figure 5. pH-impédancemétrie œsophagienne des 24 heures (pHi). Exemple de tracé.
La pH-impédancemétrie œsophagienne des 24 heures (pHi) est considérée comme l’examen de référence du diagnostic paraclinique du RLP(13).
Il faut distinguer la pHi de la pH-métrie œsophagienne des 24 heures, pratiquée avec une seule électrode à pH positionnée au niveau du bas œsophage et sans impédancemétrie associée, car cet examen mésestime le RLP et n’est donc pas pertinent en ORL. Sur une même sonde sont couplées deux électrodes à pH (distantes généralement de 15 cm) et 8 électrodes à impédance disposées autour des électrodes à pH. La sonde est introduite par voie nasale et connectée à un boîtier enregistreur pendant 24 heures. Le pH-mètre proximal est placé à 15 cm de l’orifice narinaire, soit au niveau du sphincter supérieur de l’œsophage, et le pH-mètre distal à 5 cm de l’orifice hiatal. La sonde est connectée à un boîtier enregistreur porté en bandoulière. Les périodes de repas, de coucher, et les événements significatifs sont renseignés par le patient pendant l’examen. Le traitement par IPP est généralement interrompu pendant les 8 jours précédant l’examen. L’activité du patient et son régime alimentaire doivent être le plus proche possible de ses habitudes. La survenue d’un reflux proximal (pharyngé) est un événement relativement rare et donc très significatif, si bien que le RLP est affirmé par la survenue de 2 événements, au mois, de reflux proximal(14). Il peut être acide, ou peu/non acide, liquide ou gazeux, et seule la pHi peut alors le mettre en évidence.
L’examen, parfois désagréable, est généralement bien toléré, en s’aidant pour la mise en place de la sonde d’une anesthésie locale légère. Les complications sont rares(15).
La pHi est prise en charge par l’Assurance maladie (HEQD002 + HQQP001/2 soit 116,02 €), mais reste peu diffusée en France auprès des ORL, car consommatrice de temps pour son installation et son interprétation, et du fait du coût relativement élevé de la sonde.
Dosage de la pepsine salivaire (Peptest®)
(figure 6)
Figure 6. Dosage de la pepsine salivaire Peptest®. Test immuno-chromatographique spécifique de la pepsine 3. La salive est recueillie le matin à jeun et le soir après le dîner. Le test est positif si > 36 ng/mL et franchement positif si > 75 ng/mL.
Le Peptest® est un test salivaire rapide(16) qui dose par immunochromatographie l’isoenzyme 3 b, le plus répandu, de la pepsine dans la salive. Un lecteur chromatographique (Cube Reader) mesure le taux de pepsine exprimé en ng/mL.
Deux recueils salivaires sont réalisés : le matin à jeun et le soir après le dîner. Le seuil de positivité est de 16 ng/mL selon le fabricant, mais il apparaît plus pertinent en clinique de retenir le seuil de 36 ng/mL comme positif et de 75 ng/mL comme franchement positif.
Le taux de pepsine n’est pas corrélé directement au reflux mesuré par pHi mais est influencé par l’alimentation consommée dans les heures précédant la collection salivaire.
Le Peptest®, bien que n’étant pas pris en charge par l’Assurance maladie, se diffuse progressivement auprès des laboratoires d’analyses biologiques.
pH-métrie pharyngée (Restech®)
(figures 7 et 8)
Figure 7. pH-métrie pharyngée Restech®. Mise en place de la sonde et du boîtier enregistreur.
Figure 8. pH-métriepharyngéeRestech®. Exemple de tracé.
La pH-métrie pharyngée(17) (Restech®) mesure pendant 24 heures l’acidité oropharyngée. Une fine sonde introduite par voie nasale présente à son extrémité une électrode à pH originale, fonctionnelle dans un environnement légèrement humide et dont la fréquence d’analyse est élevée (2 mesures par seconde). La sonde est connectée à un transmetteur luimême en relation non filaire avec un boîtier enregistreur. L’extrémité de la sonde est positionnée au niveau du bord postérieur du voile du palais en s’aidant d’une diode clignotante.
La courbe obtenue est évaluée par rapport au pH par tranche de 0,5 entre le pH 6,5 et plus et le pH 5,5 et moins(18).
Le RLP acide est mesuré par quantification de la courbe d’enregistrement dans chaque tranche de pH, en période diurne et nocturne, et évalué par rapport aux normes établies en position debout et couchée (score de Ryan).
Le RLP non acide est objectivé indirectement lorsque des variations très marquées d’amplitude de la courbe d’enregistrement sont observées dans la zone de pH supérieur à 6,5.
La pH-métrie pharyngée Restech® est relativement facile à réaliser, assez bien tolérée, et adaptée à l’activité ORL, mais elle n’est pas remboursée en France par l’Assurance maladie (à la différence du Luxembourg par exemple), ce qui limite sa diffusion.
PRISE EN CHARGE(9,10)
Lorsque les critères diagnostiques du RLP sont réunis (RSS > 13 ou RSS-12 > 11 et RSA > 14), le diagnostic clinique peut être retenu, mais ne sera confirmé que par la réalisation d’une pH-impédancemétrie des 24 heures.
Dans le cas où le patient rapporte des symptômes légers, une diète anti-reflux(21) peut être suffisante, mais doit être associée à la gestion du stress du patient, pendant 6 à 12 semaines ; durée nécessaire pour obtenir une guérison des lésions. En cas de tableau clinique plus invalidant, la réalisation d’une pH-impédancemétrie de 24 heures peut être nécessaire et permettra de préciser les caractéristiques du RLP : acide, faiblement acide, non acide, RGO associé (DeMeester score > 14,7), moment de sur venue de s épisodes de reflux (diurne, nocturne) et de prescrire un traitement adéquat associant régime, gestion du stress et certains des médicaments suivants : inhibiteurs de la pompe à protons (IPP), alginates.
Quel que soit le traitement, le RSS permet d’apprécier l’évolution clinique à trois mois et de titrer/adapter les doses de médicaments.
En cas de RLP non-acide, on propose pendant 6 à 12 semaines des pansements gastriques à base d’alginate, après chaque repas, associés aux règles hygiéno-diététiques (figure 9).
Figure 9. Règles hygiéno-diététiques du RLP (et du RGO). Fiche de conseils hygiéno-diététiques avec un schéma des voies digestives supérieures servant de support pédagogique. Le café, le thé, le tabac et l’alcool sont très refluxogènes, ainsi que les graisses.
En cas de RLP acide ou peu acide, on propose un traitement par IPP en une ou deux prises (20 mg), matin et/ou soir, une demi-heure avant le repas. La durée d’action d’un IPP oscille entre 6 et 18 heures. En cas de reflux diurne, une dose de 20 mg (ou 15 mg si lansoprazole) le matin peut être suffisante.
Le Peptest® et le Restech® peuvent être proposés comme alternative à la pHi, lorsque cet examen est indisponible. La fibroscopie digestive sera proposée en fonction de l’âge et du terrain, et/ou lorsqu’un RGO est associé.
Le traitement chirurgical du reflux cible surtout le RGO associé au RLP(22) et ne présente que peu d’impact surles symptômes de RLP.
CONCLUSION
• Le RLP est fréquemment évoqué, mais difficile à diagnostiquer.
• Les scores RSS et RSA aident au diagnostic et au suivi.
• La pHi et/ou la pH-métrie pharyngée Restech® sont performants, mais peu disponibles en France.
• Le Peptest® est utile, mais il n’est pas pris en charge par l’Assurance maladie.
• La place du test pragmatique par IPP, trop facilement proposé, et contesté par la HAS, doit être réévaluée et validée par les examens disponibles.
• À l’inverse, les pansements digestifs à base d’alginate, l’alcalinisation locale et les règles hygiéno-diététiques sont des mesures utiles et sans danger.
Liens d’intérêt : aucun.
Références sur demande à la rédaction : biblio@len-medical.fr
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :