Dermato - Allergo
Publié le 11 oct 2015Lecture 10 min
Les biomédicaments dans l’urticaire chronique et la dermatite atopique
D. STAUMONT-SALLE, hôpital Claude-Huriez, CHRU Lille - Université Lille 2 Inserm U1011, Institut Pasteur de Lille
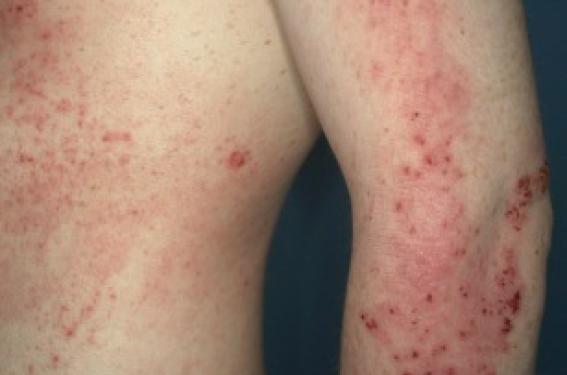
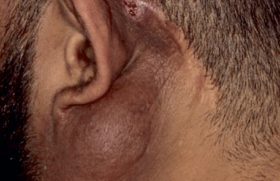
La dermatite atopique et l’urticaire chronique spontanée sont des affections chroniques pouvant avoir un impact important sur la qualité de vie du patient et de son entourage. Dans la grande majorité des cas, les traitements de référence sont efficaces, qu’il s’agisse des anti-H1 non sédatifs pour l’urticaire chronique et des dermocorticoïdes pour la dermatite atopique. Cependant, ces traitements de première intention peuvent parfois être inefficaces et d’autres solutions thérapeutiques doivent alors être trouvées pour ces patients très gênés dans leur vie quotidienne.
Les biomédicaments font désormais partie de l’arsenal thérapeutique dans l’urticaire chronique spontanée réfractaire aux anti-H1, avec l’obtention en février 2014 d’une autorisation de mise sur le marché de l’omalizumab (anticorps monoclonal anti-IgE) dans cette indication. À l’heure actuelle, aucun biomédicament n’est disponible pour la dermatite atopique, mais plusieurs molécules ciblant des mécanismes immunologiques soustendant la pathologie sont en cours de développement, avec des résultats préliminaires prometteurs. La dermatite atopique (DA) et l’urticaire chronique spontanée (UCS) sont deux dermatoses inflammatoires fréquentes. En effet, la DA affecte près de 25 % des enfants et 3 à 5 % des adultes (figure 1) dans les pays occidentaux. Environ 1 % de la population générale est concernée par l’UCS (figure 2). Chez l’adulte en particulier, et dans les cas les plus sévères, il n’est pas rare de se trouver en situation d’échec avec les traitements dits « conventionnels ». La prescription de traitements immunosuppresseurs peut alors être envisagée, mais leur mode d’action n’est pas spécifique de l’affection et leur utilisation non dénuée d’effets indésirables. Le recours à des thérapies davantage ciblées sur la physiopathologie, comme les biomédicaments, offre l’avantage de combiner une plus grande efficacité thérapeutique à une meilleure tolérance. La révolution thérapeutique que nous avons connue avec l’arrivée des biomédicaments dans le psoriasis nous incite à porter notre espoir dans le développement de ces derniers dans l’UCS et la DA. Figure 1. Dermatite atopique sévère de l’adulte. Figure 2. Urticaire chronique spontanée (UCS). Le présent : biomédicaments dans l’urticaire chronique En cas d’urticaire chronique spontanée (UCS) résistante à un traitement par antihistaminique (anti-H1) de seconde génération bien conduit (anti- H1 prescrit à la posologie de l’AMM, de manière quotidienne, en pratique pendant au moins 4 à 6 semaines), il est recommandé par les conférences de consensus de 2009 et de 2012 d’augmenter la dose journalière des anti-H1 jusqu’à 4 fois(1). Moins d’un quart des malades ne répondra pas aux anti-H1 quelle que soit la posologie. Il faudra alors envisager d’autres lignes thérapeutiques pour ces malades dont la qualité de vie est considérablement altérée. Les options sont alors multiples : antileucotriènes (montelukast), drogues anti-inflammatoires (colchicine, disulone, etc.), immunosuppresseurs (ciclosporine, méthotrexate). Mais il s’agit de prescriptions hors AMM, avec un niveau de preuve scientifique relativement faible, des résultats aléatoires et une tolérance parfois médiocre. Le recours aux biomédicaments constitue donc une approche thérapeutique d’intérêt pour ces malades présentant une UCS réfractaire aux anti-H1. Omalizumab L’omalizumab (Xolair®) est un anticorps (Ac) monoclonal IgG1 humanisé dirigé contre l’IgE, qui a l’AMM dans l’asthme allergique sévère de l’enfant et de l’adulte. Il a obtenu une AMM européenne en février 2014 dans l’indication « UCS sévère résistante aux anti-H1 ». Sa commercialisation effective est prévue courant 2015. Dès 2008, de nombreux cas cliniques et des petites séries ont témoigné de l’efficacité de l’omalizumab dans de nombreuses formes cliniques d’UC : UCS avec ou sans auto-immunité, angiooedème histaminique, urticaires physiques dont urticaire au froid(2). L’efficacité et la bonne tolérance de l’omalizumab dans l’UCS ont ensuite été confirmées dans plusieurs études multicentriques contrôlées contre placebo(3-5). La posologie recommandée dans l ’UCS est de 300 mg, en administration souscutanée. Une adaptation de la posologie au taux d’IgE sérique n’est pas utile dans l’UCS, contrairement à ce qui est fait dans l’asthme. En effet, l’omalizumab peut être efficace dans l’UCS, même si le taux d’IgE n’est pas élevé, ce qui suggère un mode d’action de l’omalizumab en partie indépendant de l’IgE. L’étude du profil de tolérance au cours des études contrôlées n’a révélé aucun nouveau signal chez les malades atteints d’UCS comparativement aux malades asthmatiques. Une étude rétrospective récente menée en Espagne conforte l’efficacité de l’omalizumab dans la pratique courante, avec une réponse complète ou significative chez 80 % des patients(6). Les limites du traitement par omalizumab sont représentées par son caractère souvent suspensif et son coût élevé. Les modalités de prescription de l’omalizumab dans le cadre de l’AMM sont encore en cours de définition (fréquence des injections, durée du traitement). Autres biomédicaments Il s’agit d’indications exceptionnelles rapportées de manière ponctuelle dans la littérature, non confirmées par des études contrôlées et/ou à plus grande échelle : immunoglobulines polyvalentes, rituximab (Ac monoclonal anti-CD20, ayant pour cible la réponse lymphocytaire B), étanercept (anti-TNF). Le futur proche : biomédicaments dans la dermatite atopique En cas de DA sévère de l’adulte ou de l’adolescent réfractaire à un traitement topique bien conduit (associant dermocorticoïdes et émollients), il est classique d’avoir recours à des traitements immunosuppresseurs dont l’action n’est pas spécifique des mécanismes immunologiques sous-tendant la DA. Ces médicaments, tels la ciclosporine, le méthotrexate, l’azathioprine ou le mycophénolate mofétil, exposent le malade à des complications liées à l’immunosuppression induite ou à une toxicité propre à chaque molécule. Aucun biomédicament ne dispose d’une AMM dans la DA à l’heure actuelle. La plupart des biomédicaments dont l’utilisation dans la DA sévère a été rapportée dans la littérature sont des molécules ayant été développées pour d’autres maladies inflammatoires, en particulier le psoriasis ou l’asthme. Ces biomédicaments vont cibler les différents mécanismes immunologiques sous-tendant la physiopathologie de la DA(7). Thérapie ciblant l’IgE : omalizumab Les résultats obtenus avec l’omalizumab dans la DA réfractaire aux traitements conventionnels sont globalement décevants(8). L’omalizumab semble être davantage efficace en cas de DA associée à un asthme. Thérapie ciblant le lymphocyte B : rituximab L’analyse des quelques petites séries ou case reports publiés dans la littérature fournit des résultats contradictoires concernant l’efficacité du rituximab dans la DA. Des études contrôlées seront nécessaires pour valider ou non l’intérêt de ce biomédicament dans la DA. Thérapies ciblant la réponse Th2 Thérapies anti-IL-4 Plusieurs inhibiteurs de l’IL-4 et de ses voies de signalisation sont en cours de développement dans l’asthme et dans la DA(9). Le dupilumab (REGN668), Ac monoclonal dirigé contre le récepteur de l’IL-4, a fait la preuve de son efficacité dans la DA de l’adulte dans des essais de phase 1 et 2, et un essai de phase 3 devrait bientôt débuter. Le pascolizumab (SB 240683), Ac monoclonal humanisé dirigé contre l’IL-4, s’est révélé efficace dans des essais cliniques de phase 1 et 2 dans l’asthme, mais il n’a pas encore été testé dans la DA. Le pitrakinra est un antagoniste de la sous-unité du récepteur de l’IL-4, il s’agit donc stricto sensu d’une petite molécule et non d’un biomédicament. Son effet thérapeutique potentiel (par injection sous-cutanée ou par inhalation) a été confirmé dans des essais cliniques de phase 1 et 2 dans l’asthme. Des résultats préliminaires encourageants ont été observés chez des malades atteints de DA traités par injection sous-cutanée de pitrakinra dans une étude de phase 2. Thérapies anti-IL-5 Le mépol izumab est un Acmonoclonal humanisé dirigé contre l’IL-5, utilisé dans le cadre d’essais cliniques dans les syndromes hyperéosinophiliques. Bien qu’il réduise significativement le nombre d’éosinophiles circulants et cutanés chez les malades atteints de DA, le mépolizumab se révèle peu efficace sur le plan cl inique dans cet te pathologie(10). Autres thérapies anti-IL-2 Elles sont en cours de développement : antagonistes de l’IL- 31, cytokine clé du prurit (en phase 1 dans la DA) ; antagonistes de la TLSP, chimiokine jouant un rôle essentiel dans l’induction de la réponse inflammatoire cutanée (en phase 1 dans la DA). Thérapies ciblant la réponse Th1 Le principe de cette stratégie thérapeutique dans la DA est d’apporter, dès la phase aiguë de la maladie, de l’IFN-recombinant (Th1) afin de restaurer l’équilibre Th1/Th2 et diminuer la réponse IgE. Le traitement par IFN n’a cependant été efficace que chez un nombre limité de malades atteints de DA. Thérapies ciblant les réponses TNF et Th17 Anti-TNF Grâce à son action synergique avec l’IL-17, le TNF est une autre cible thérapeutique potentielle dans la DA. La manipulation désormais aisée dans le psoriasis des Ac monoclonaux dirigés contre le TNF (infliximab, adalimumab) ou d’une protéine de fusion bloquant le récepteur du TNF-�gamma (étanercept) a favorisé l’essai de ces molécules chez des malades atteints de DA modérées à sévères. L’infliximab a été prescrit chez des adultes dans le cadre d’une étude pilote et l ’étanercept chez deux enfants, l’étanercept disposant d’une AMM dans le psoriasis de l ’enfant . Une amélioration clinique a été observée pour la majorité des malades traités, mais avec une réponse thérapeutique trop cour te pour conclure à une efficacité des anti-TNF dans ces observations. Anti-IL-12/IL-23 (ustekinumab) Il convient donc de viser une cible plus précise que le TNF dans la DA. L’IL-23 est une cytokine essentielle pour la différentiation des lymphocytes Th17 producteurs d’IL-17. L’inhibition sélective de la voie de signalisation IL-12/IL-23 peut donc avoir un intérêt thérapeutique dans la DA, comme dans le psoriasis. L’ustekinumab, Ac monoclonal dirigé contre la sous-unité p40 commune à l’IL- 12 et à l’IL-23, dispose d’une AMM dans le psoriasis. Son efficacité dans la DA a récemment été rapportée, mais des études complémentaires seront nécessaires pour confirmer l’intérêt de cette molécule dans la DA. l Anti-IL17 La mise à disposition prochaine dans le psoriasis de biomédicaments ciblant spécifiquement l’IL-17 (comme l’ixekinumab et le brodalumab, Ac monoclonaux dirigés respectivement contre l’IL-17 et le récepteur de l’IL-17) devrait conduire à l’essai de ces molécules dans la DA. En pratique Quelles que soient la molécule et l’indication, les règles générales d’utilisation des biomédicaments devront être respectées : – identifier le patient éligible, atteint d’une pathologie sévère réfractaire aux traitements de référence bien conduits, et valider l’indication en réunion de concertation ; – respecter la balance bénéfice/ risque et le cas échéant réaliser scrupuleusement le bilan préthérapeutique recommandé ; – identifier le patient répondeur, si possible à l’aide de biomarqueurs ; – prendre en compte l’impact médico-économique de la prescription d’une molécule coûteuse.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :