ORL
Publié le 15 mar 2021Lecture 10 min
Les dysphonies de l’enfant
Denis GALLAS, Groupe hospitalier du Sud de l’Oise, Senlis
La prévalence des dysphonies de l’enfant en âge scolaire varie de 0 à 38 % selon les séries, surtout lorsqu’elles concernent des groupes particulièrement sensibilisés à la qualité vocale (choeur d’enfants). Le pic de fréquence se situe entre 8 et 10 ans (44 %), avec 30 % d’enfants de moins de 7 ans. Il existe une prédominance masculine avant l’âge de 10 ans, puis féminine après l’âge de 13 ans.
La demande de consultation émane rarement de l’enfant (1 %), qui la tolère généralement bien, de l’entourage proche dans 40 %, et de personnes extérieures à la famille dans 59 % (médecin, orthophoniste, enseignant en musique ou en chant, éducateur sportif).
Cette pathologie est dominée par la pathologie fonctionnelle, mais peut révéler une lésion organique sous-jacente. La dysphonie survient sur un larynx en croissance, avec des lésions se modifiant avec l’âge.
L’anatomie du larynx du nourisson
Le larynx de l’enfant n’est pas un larynx adulte de volume réduit. C’est un organe en croissance régulière avec deux périodes d’accélération de croissance importante : entre la naissance et 2 mois, puis à la puberté. Il est haut situé à la naissance, presque au niveau de la langue, avec le cartilage cricoïde situé en regard de C3, très incliné vers le bas et l’arrière. L’épiglotte vient ainsi recouvrir le voile du palais (plus long chez le nourrisson, avec une base de langue plus volumineuse) créant deux voies séparées : l’une respiratoire directe du nasopharynx jusqu’au poumon, l’autre digestive latérale via les amygdales, les sinus piriformes et l’oesophage. Ainsi, la respiration du nourrisson jusqu’à 4 mois est-elle quasi exclusivement nasale.
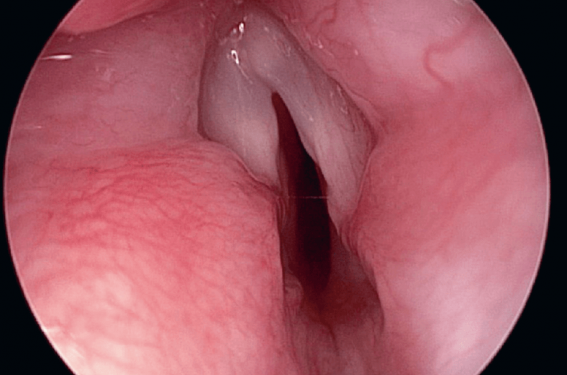
Le larynx du nourrisson (figure 1) est tronconique avec la plus petite section au niveau de la sous-glotte (5 mm chez le nouveau-né) avec un tissu conjonctif lâche, ce qui favorise la constitution d’oedème et la survenue de dyspnée (laryngite, intubation traumatique…). Un oedème de 1 mm réduit alors le débit aérien de 80 %.
Figure 1. Larynx du nourrisson (avec paralysie récurrentielle gauche en adduction séquellaire de chirurgie cardio-thoracique [canal artériel]).
La sous-glotte y est plus étroite que la trachée. L’épiglotte est proportionnellement plus développée, plus enroulée que chez l’adulte (en oméga majuscule), plus flaccide, ce qui peut gêner l’examen du plan glottique, et favoriser l’invagination des structures sus-glottiques en inspiration, notamment en cas de laryngomalacie. Les bandes ventriculaires sont plus épaisses et plus larges. Les étages glottiques et sous-glottiques sont plus ovalaires que chez l’adulte. Au plan glottique, les aryténoïdes sont plus volumineux, et les apophyses vocales plus antérieures que chez l’adulte. La taille des plis vocaux est de 4,5 mm à la naissance.
La phonation du nourrisson survient dans un régime de pression sous-glottique élevé, avec des cordes vocales structurellement impropres à la phonat ion : la corde vocale est composée histologiquement d’un épithélium et d’une lamina propria sans espace de Reinke, ni ligament vocal. La phonation lors du premier cri serait en rapport avec une pression élevée sous-glottique, avec effet Venturi au niveau de l’espace sous-glott ique (le plus étroit) et fermeture du plan glottique puis ouverture ou fermeture des bandes ventriculaires, le tout dans un faible flux d’air (capacité vitale pulmonaire du nourrisson faible et respiration abdominale). La durée du cri est de l’ordre de 1 seconde avec une fondamentale autour de 500 Hz et de nombreuses harmoniques aiguës autour de 3 000 Hz.
Modifications topographiques du larynx
Avec la croissance, apparaît un élargissement du pharynx, une descente de la langue vers le pharynx, et surtout une descente du larynx dans le cou. Cette dernière est fondamentale pour la production de la parole. Ainsi l’os hyoïde se projette-t-il en regard de C3 à la naissance, de C4 à 1 an, de C5 à 2 ans, de C6 après 5 ans (figure 2).
Figure 2. Descente du larynx. (A) à la naissance (flèche du haut) et à 2 mois (flèche du bas). (B) à 18 mois (flèche du haut) et à 13 ans (flèche du bas).
La croissance du larynx se fait dans toutes les dimensions, avec une augmentation plus importante de la corde vocale qui représentait moins de la moitié du plan glottique chez le nouveau- né, et qui représente les deux tiers après 10 ans (comparaison figure 1 et figure 3).
Figure 3. Larynx grand enfant normal.
Le pli vocal évolue histologiquement progressivement de 6 à 15 ans vers une structure trilamellaire pour arriver à une structure de type adulte à 17 ans : couche superficielle lâche et décollable (espace de Reinke), couche intermédiaire élastique, couche profonde plus rigide (ligament vocal). Il s’allonge (17 à 23 mm chez le garçon, 13 à 17 mm chez la fille) et s’épaissit.
Les résonateurs évoluent progressivement : diminution relative du volume lingual, désenclavement vélo-pharyngé lors de la descente du larynx, élargissement des cavités oro- et rhino-pharyngées, élargissement des fosses nasales et pneumatisation des cavités sinusiennes.
À la puberté, l’accélération de la croissance du larynx sous l’effet des hormones sexuelles est plus importante chez le garçon que chez la fille. L’angle thyroïdien reste ouvert chez la fille à 120°, et 90° chez le garçon (saillie de la pomme d’Adam). La cage thoracique se développe avec maturation pulmonaire se terminant vers 18-20 ans.
La hauteur moyenne de la voix diminue en fonction des évolutions anatomiques :
3 ans : 320 Hz ;
4-5 ans : 280-300 Hz ;
6-7 ans : 250-270 Hz ;
11 ans : 240-260 Hz garçon/ 250-270 Hz fille ;
adulte : 120-240 Hz garçon/ 220-250 Hz fille.
Démarche diagnostique
L’interrogatoire des parents recherche :
• la date de début
• le mode d’accouchement et la qualité du premier cri
• le caractère permanent ou intermittent
• les antécédents d’intubation ou de traumatisme laryngé
• les antécédents de chirurgie cervicale ou thoracique
• les antécédents d’allergie, de pneumopathies, de fausses routes
• la qualité du développement psycho-moteur
• les anomalies associées
• la présence d’une dysphonie dans la famille, en particulier chez les parents
• la présence d’un environnement bruyant familial, avec habitude de parler fort
• l’existence d’une famille nombreuse et la position de l’enfant dans la fratrie
• la pratique d’activités extrascolaires (sports, surtout collectifs, musique, chant…)
• le caractère intro- ou extraverti de l’enfant
• le retentissement personnel de la dysphonie (important dans la décision thérapeutique)
• la qualité de la voix et des pleurs : raucité (pathologies glotto-sousglottiques), voix éteinte (palmures et sténoses glottiques), voix bitonale (paralysies laryngées), voix couverte pathologie sus-glottique ou obstacle pharyngé)
• l’existence d’un bruit respiratoire intermittent : prédominance à l’effort (tétée et pleurs chez le nourrisson) orientant vers un obstacle fixe, ou lors du sommeil (laryngomalacie, trachéomalacie, pathologies neurologiques)
• l’existence d’une toux à distance ou lors des prises alimentaires, éventuellement accompagnées de dyspnée, malaise, cyanose, et leur circonstances déclenchantes
• l’existence de signe de reflux gastro-oesophagien
L’ inspection de l’enfant recherche :
• un trouble maxillo-facial
• un stridor
• un ronflement
• un cornage
• d’éventuels signes de gravité respiratoire
L’écoute de la voix est évaluée le plus souvent par l’échelle GRBASI (cotée de 0 = normal à 3 = atteinte sévère) : Grade = aspect général, Roughness = raucité, Brethyness = aspect voilé, Asthenicity = manque d’harmoniques aiguës, Strained = forçage, Instability = variabilité.
L’examen clinique ORL vérifie l’absence de dérèglement de la boucle audio-phonatoire par une cause indolore et méconnue de surdité (bouchon de cérumen, otite séreuse…).
Il est complété par une nasofibroscopie (ou suivant les habitudes de l’opérateur, fibroscopie par voie buccale possible avant l’éruption des premières dents) sans franchissement du plan glottique (risque de spasme ou d’oedème).
En fonction de l’âge, de la compliance de l’enfant et de l’expérience de l’ORL, un examen à l’épipharyngoscope (optique rigide à 70° ou 90°) peut être réalisé (figure 4). Il est le seul à pouvoir être couplé à une stroboscopie.
Figure 4. Épipharyngoscopie.
En fonction des lésions retrouvées ou de l’absence de lésion retrouvée expliquant les symptômes, l’examen sera complété par une laryngo-trachéoscopie sous anesthésie générale au bloc opératoire dans un contexte anesthésique entraîné, en ventilation spontanée dans un premier temps. Elle peut permettre aussi un geste opératoire adapté aux lésions. Dans ce cas, le respect de la lamina propria des cordes vocales est impératif.
Les principaux tableaux cliniques avant 6 mois
La laryngomalacie
Collapsus des structures supraglottiques à l’inspiration, cause la plus fréquente de stridor, elle est favorisée par l’anatomie du larynx du nourrisson : épiglotte tubulée flaccide, basculant en arrière, replis ary-épiglottiques flaccides et oedémateux, souvent plus courts, bascule vers l’avant des aryténoïdes à l’inspiration (figure 5). Elle se manifeste par un bruit inspiratoire de tonalité aiguë aggravé aux pleurs et à l’alimentation. Fréquemment associée à un reflux gastro-oesophagien auto-entretenu par le collapsus. Augmente fréquemment entre 0 et 4 mois et régresse fréquemment après l’âge de 1 an.
Figure 5. Laryngomalacie avec replis ary-épiglottiques courts, flaccides aspirés vers le plan glottique en inspiration.
La paralysie laryngée
Seconde cause de stridor, aigu avec voix normale ou bitonale, et fausses routes minimes. Étiologies congénitales malformatives (neurologiques centrales, cardiovasculaires), génétiques, acquises (traumatiques obstétricales ou chirurgie cardio-pédiatrique, infectieuses), idiopathiques. Les causes les plus fréquentes sont la chirurgie cardio- ou -thoraco-pédiatrique pour les paralysies unilatérales (donc gauches) — figure 1— et la malformation d’Arnold Chiari pour les paralysies bilatérales. Environ un tiers des paralysies est idiopathique. L’examen endoscopique sous anesthésie générale n’est pas nécessaire dans les formes unilatérales sans gravité, et l’est dans les autres formes.
L’angiome sous-glottique
Stridor de type cornage, voix rauque, toux aboyante, apparaissant après quelques semaines de vie, répondant initialement aux corticoïdes mais récidivant à l’arrêt. La prise en charge a été révolutionnée par la prise de propanolol.
La palmure glottique
Fusion de la partie antérieure des cordes vocales pouvant atteindre la lamina propria (figure 6). Considérée comme une atrésie partielle du larynx, si elle s’associe à une sténose glotto-sousglottique congénitale. Elle se manifeste par une voix absente, un stridor et une dyspnée variables selon l’importance de la palmure et/ou de la sténose sousglottique. Fréquence de la microdélétion 22q11 et des lésions associées à rechercher.
Figure 6. Palmure laryngée.
La sténose sous-glottique
Stridor de type cornage, voix rauque, toux aboyante, apparaissant dès la naissance.
Le diastème laryngé
Fausses routes et malaise au premier plan, avec pneumopathies récidivantes, dysphonie et dyspnée variables.
Les principaux tableaux cliniques après 6 mois
Les dysphonies aiguës
• Infections virales
• Forçage vocal ponctuel (match de football, concert, karaoké…)
Les dysphonies chroniques sans lésion des cordes vocales
• Aphonies (ou dysphonie) psychogènes
En général retrouvées chez l’adolescente. La toux est conservée. Une hyperkinésie des bandes ventriculaires pouvant masquer le plan glottique peut être observée. Nécessi te une pr ise en charge fonctionnelle et éventuellement psychologique pour éviter que l’hyperkinésie des bandes ventriculaires ne se chronicise.
• Troubles de la mue
Par conservation du mécanisme 2 (voix de tête ou voix de fausset), surtout chez l’adolescent post-pubère. La toux est en générale grave en mécanisme 1 (voix de poitrine). La voix est éraillée avec de fréquents changements de registre vocal. Prise en charge fonctionnelle.
Les dysphonies chroniques avec lésion des cordes vocales
En plus des lésions décrites avant 6 mois, on retrouve :
• Les lésions nodulaires
Nodule vrai le plus fréquent, en général kissing-nodules situés à la jonction tiers antérieur-tiers moyen des cordes vocales, un peu en dessous de leur bord libre. Témoigne d’un conflit dysfonctionnel (tel le cor au pied qui témoigne d’un conflit entre le chaussant et le pied). Le traitement est or thophonique, après 6 ans, et fonction de la motivation de l’enfant et de son entourage. La phono-chirurgie n’est réservée qu’aux échecs du traitement orthophonique, du contexte (chanteur…), pas avant 10 ans, encadrée par une prise en charge orthophonique préet postopératoire. À noter par ai l leurs que la plupar t des lésions nodulaires régressent après la puberté, surtout chez le garçon (figure 7).
Figure 7. Kissing-nodules.
• Les polypes, exceptionnels chez l’enfant
Les laryngopathies organiques
Probablement congénitales, dont l’origine serait commune, et dont le traitement est en principe chirurgical, pas avant 10 ans (acceptation du repos vocal postopératoire par l’enfant, entre autres).
• Kystes épidermiques
Voussure unilatérale blanchâtre du bord libre de la corde vocale, pouvant envahir le ligament vocal (figure 8).
Figure 8. Kyste épidermique de la corde vocale
• Pont muqueux
Bride muqueuse parallèle au bord libre de la corde vocale, dont elle se détache, de découverte généralement per-opératoire (figure 9). Pourrait correspondre à un kyste épidermique spontanément ouvert en deux points.
Figure 9. Pont muqueux.
• Sulcus vocalis
Invagination de l’épithélium réalisant une poche s’enfonçant jusqu’au ligament vocal (figure 10). Pourrait correspondre au résultat de la vidange spontanée d’un kyste, avec persistance du fond épithélial dans l’épaisseur de la corde.
Figure 10. Sulcus vocalis.
La papillomatose laryngée
Pathologie rare mais qui doit être absolument diagnostiquée ou éliminée, du fait de son évolution récidivante, et des difficultés thérapeutiques qui en résultent (figure 11). Liée principalement au virus HPV 6 ou 11. Probable transmission materno-foetale, certains cas étant survenus après accouchement par césarienne. Peut survenir à tout âge et entraîner dysphonie, voire dyspnée en fonction de son extension. On peut espérer à long terme une diminution d’incidence si la vaccination anti-HPV devait s’étendre. Dans sa forme de papillomatose respiratoire récidivante juvénile (âge moyen d’apparition de 4 à 5 ans), la cancérisation est rare, et l’amélioration fréquente à la puberté. Le traitement consiste en une chirurgie d’exérèse répétée (laser, microdébrideur) à visée désobstructive (souvent plusieurs par an) ± cidofovir. De multiples thérapeutiques adjuvantes ont été essayées. Un protocole réservé à quelques centres spécialisés avec du bévacizumab (Avastin®) (en coordination avec les onco-pédiatres) est en cours et pourrait être prometteur.
Figure 11. Papillomatose laryngée.
Conclusion
• La dysphonie de l’enfant est une pathologie assez fréquente, dont les pathologies acquises sont les plus fréquentes, et le traitement généralement médical et/ou orthophonique.
• Elle nécessite toutefois d‘éliminer une pathologie congénitale, ainsi qu’une papillomatose laryngée qui nécessite une prise en charge spécifique.
• Le suivi clinique ORL régulier est difficile à obtenir dans la pratique. Moins de 10 % des enfants seront pris en charge chirurgicalement, le plus souvent par des équipes spécialisées, en respectant au maximum le ligament vocal, et en opérant en 2 temps les lésions bilatérales, afin d’éviter les brides muqueuses lors de la cicatrisation, qui engendreraient une dysphonie iatrogène.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :






